来源 :医药观澜2024-08-09
今日(8月9日),中国国家药监局(NMPA)药品审评中心(CDE)官网公示,鼎成肽源生物申报的1类创新药获批临床,拟用于治疗KRAS G12D突变阳性、基因型为HLA-A 11:01的晚期实体瘤患者。根据鼎成肽源生物早先新闻稿介绍,DCTY1102注射液为一款靶向HLA-A*11:01基因型、KRAS G12D突变的TCR-T细胞治疗产品,适应症为晚期胰腺癌、结直肠癌等恶性实体肿瘤。值得注意的是,几天前(8月6日),东北制药集团股份有限公司(东北制药)宣布拟收购鼎成肽源70%的股权。
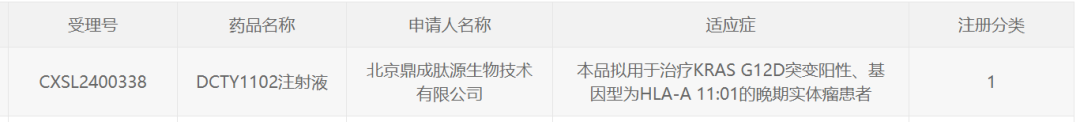 截图来源:CDE官网
截图来源:CDE官网
公开资料显示,TCR-T类细胞药物的适用人群与HLA基因型密切相关。人类白细胞抗原(HLA)系统是免疫系统重要组成部分,能将抗原肽递呈给T细胞表面的受体(TCR)。HLA-A*11:01为中国人群中表型频率较高的HLA,占比超过20%。
KRAS是常见发生突变的驱动基因,KRAS G12D是KRAS突变中主要的突变亚型,在大约34%的胰腺导管腺癌、12%的结直肠癌和4%的非小细胞肺癌以及其它多种类型癌症中可检测出。KRAS G12D突变的患者预后不佳,目前尚未有相关的靶向疗法获批上市。
就在近日(8月2日),美国FDA批准首款TCR-T细胞疗法,用以治疗某些HLA类型的晚期MAGE-A4+滑膜肉瘤成人患者,这是TCR-T疗法的重要里程碑。
本次鼎成肽源这款TCR-T细胞治疗药物获批临床,意味着该领域再次迎来新进展。
根据鼎成肽源官网介绍,该公司成立于2014年3月,聚焦免疫细胞治疗产品研发和成果转化。鼎成肽源公司围绕靶点发现、序列发现、序列评价和功能增强等环节,搭建独立自主的核心技术平台,进行TCR-T、TCR蛋白药和CAR-T细胞治疗产品的开发。

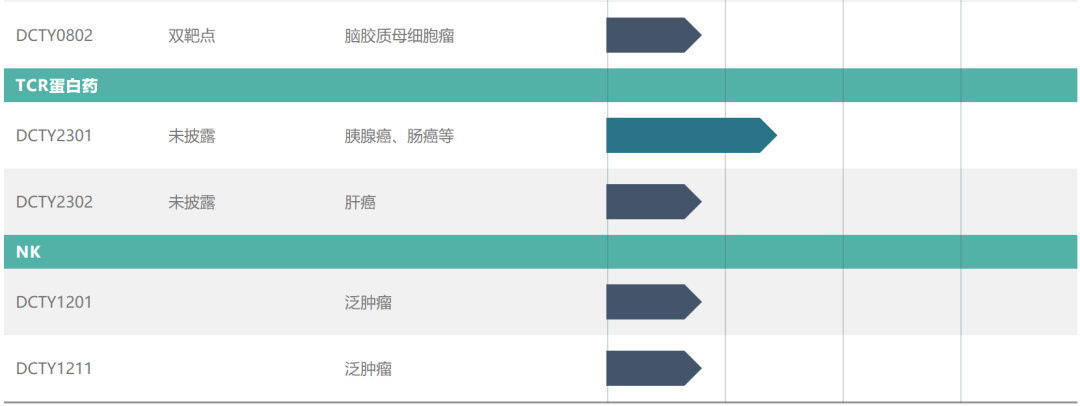 截图来源:鼎成肽源官网
截图来源:鼎成肽源官网
目前,鼎成肽源官网披露的管线产品包含10款TCR-T、TCR蛋白药、CAR-T细胞治疗产品和NK细胞治疗产品,适应症涵盖多种类型的肿瘤。其中,除了本次获批IND的DCTY1102注射液,其他进展较快的产品包括靶向EGFRvIII的CAR-T细胞治疗产品,已经进入IND申报阶段,拟开发用于脑胶质母细胞瘤。
参考资料:
[1]中国国家药监局药品审评中心官网. Retrieved Aug 9, 2024, from https://www.cde.org.cn/main/xxgk/listpage/da6efd086c099b7fc949121166f0130c
[2]鼎成肽源官网. From https://www.taiyuanshengwu.com/index.html
[3]东北制药拟收购鼎成肽源70%股权. Retrieved Aug 6, 2024, from https://mp.weixin.qq.com/s/jjLeQJgp02vlhhgvD4eNcA
本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权及其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。