报告摘要
布局“中药+化学仿制药+创新药”,用创新引领企业发展
生药业始创于1979年,于2009年深交所挂牌上市。公司以医药制造为核心主业,坚持研发创新是第一生产力,主营业务涵盖中成药、化学药、中药材、中药饮片、化学原料药的研发、生产和销售以及眼科相关产业投资,逐渐形成以创新药为发展龙头、中成药为业务基石、化学仿制药为有益支撑的可持续发展业务体系。2024年公司业绩承压触底,2025年经营恢复向好。
坚持以中药为基,化学仿制药为有益支撑
中成药是公司核心业务基础和重要增长来源,已形成覆盖眼科、心脑血管、内分泌、呼吸、清热祛湿等治疗领域的特色产品管线,主要产品包括复方血栓通系列产品(核心品种)、脑栓通胶囊(核心品种)、复方丹参片、众生丸系列产品、清热祛湿颗粒等。公司重点推动院内集采产品渠道下沉、构建零售业务培育核心品类、提升原有小份额产品市场贡献,在多产品运营策略下,稳固基本盘,提升公司经营业绩。化学仿制药是公司经营的有益支撑,产品主要覆盖呼吸、抗生素、抗病毒、抗结核、消化、眼科、抗过敏等主要治疗领域,通过专科化布局、一致性评价推进和成本优化在集采环境下保持经营韧性。
创新药管线聚焦减重、MASH、流感等多个热门治疗领域,已逐步迈入商业化兑现阶段
公司创新药布局专注于呼吸系统和代谢疾病领域,两款创新药来瑞特韦片、昂拉地韦片已进入商业化阶段,多个创新药项目处于临床试验阶段。主要在研创新药包括:1)RAY1225:GLP-1/GIP双重受体激动剂,已启动III期临床试验,在国内GLP-1多靶点减肥药中研发进度相对靠前,具备长效、低剂量、安全性好的优势,具备海外BD潜力;2)ZSP1601:国内首个获批临床用于治疗代谢功能障碍相关脂肪性肝炎(MASH)的一类创新药,处于IIb期临床试验阶段。
目录



正文
1.布局“中药+化学仿制药+创新药”,用创新引领企业发展
1.1.覆盖领域丰富,以研发创新为第一生产力
以医药制造为核心主业,坚持研发创新是第一生产力。众生药业始创于1979年,于2009年深交所挂牌上市,是一家集药品研发、生产和销售为一体的中国医药工业百强企业。公司主营业务涵盖中成药、化学药、中药材、中药饮片、化学原料药的研发、生产和销售以及眼科相关产业投资,产品覆盖心脑血管、呼吸、眼科、消化等疾病领域,以“中药为基、创新引领,聚焦特色的医药健康企业”为中期战略定位,逐渐形成以创新药为发展龙头、中成药为业务基石、化学仿制药为有益支撑的可持续发展业务体系。

公司旗下子公司业务覆盖医药制药、贸易、创新研发等板块。公司通过收并购和设立子公司拓展业务领域,从原料药到制剂生产、GAP药材种植到中药饮片与中成药生产,到健康服务生态链、创新药平台建设,逐渐形成众生特色产业链体系。制药方向子公司包括华南药业、逸舒制药、先强药业,主要负责中成药、化学药及原料药、高端辅料生产;研发方向子公司为众生睿创,是创新药研发及商业化平台;贸易公司为众生医贸,为集团营销资源整合管理平台;另设益康药业作为中药材、中药饮片及中药大健康产业平台。
1.2. 2024年业绩相对触底,2025年起经营恢复向好
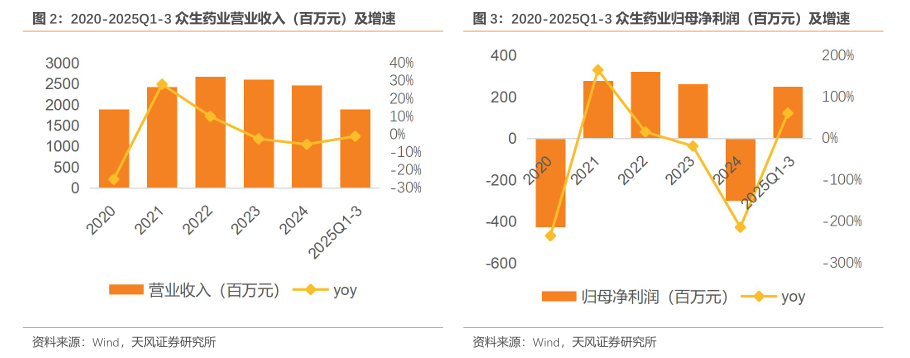
业绩受集采影响承压,2025年起企稳修复。2020-2024年公司营收和归母净利润均呈现先升后降的趋势。2024年实现营收24.67亿元(同比下滑5.48%),2024年归母净利润端由于2024年资产减值损失5.47亿元影响导致亏损2.99亿元。2025Q1-3公司营收企稳,利润回升,业绩有望持续修复。
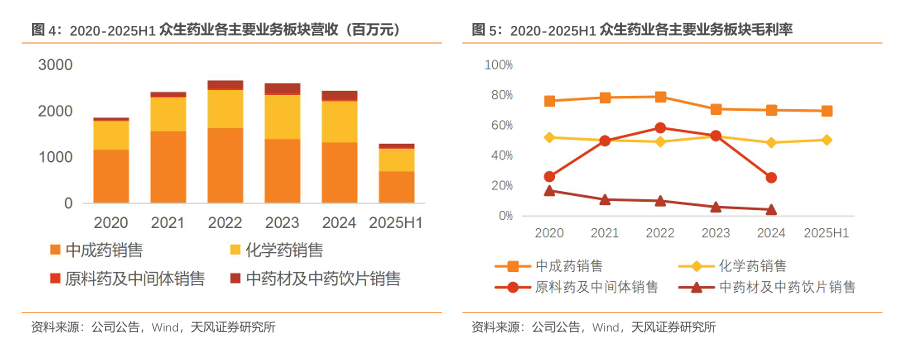
营收主要来自中成药和化学药销售,高毛利中成药占比最高。按产品的营收结构看,公司收入主要来源于中成药和化学药板块。中成药毛利率水平相对最高,23-25H1基本稳定在70%左右;25H1化学药毛利率为50.29%。
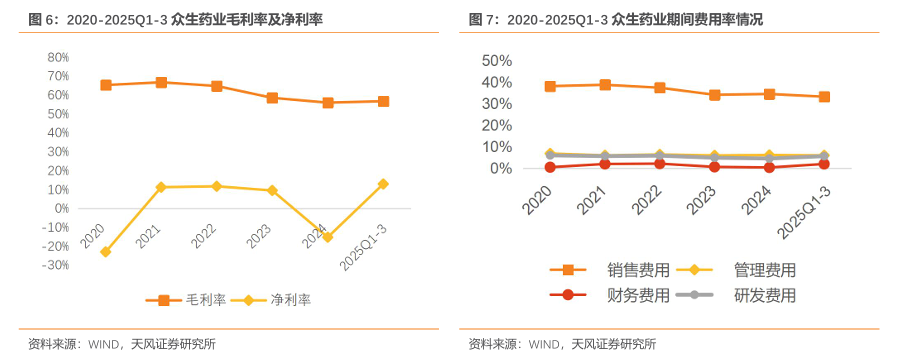
2025Q3盈利能力转好,控费效果显著。毛利率从2020年的65.34%下滑至2024年的56.03%;净利率从2020年-22.92%恢复至2021年11.31%,2023年下滑至9.57%。2025年Q3毛利率及净利率均现企稳迹象。2020-2025Q3期间费用率整体呈下降趋势,从2020年的51.43%下降至2025Q3的46.82%,费用控制逐步优化,尤其是销售费用率下降明显,从2020年的38.10%下降至2025Q3的33.20%。
1.3.推出员工持股计划激励创新药研发
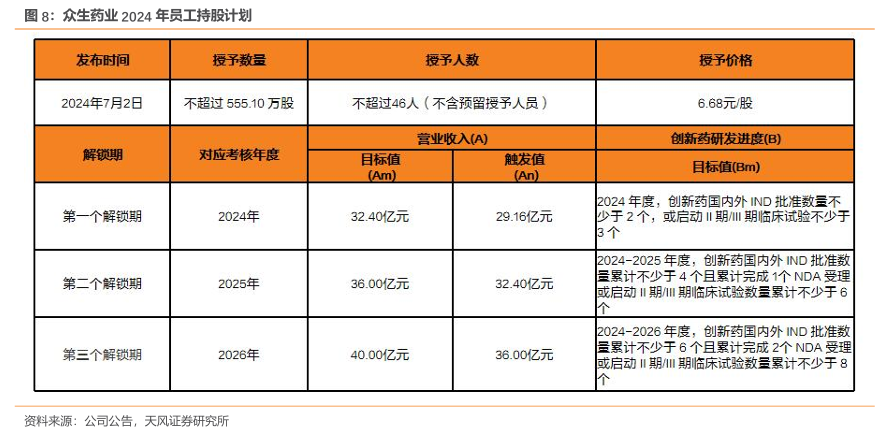
推出2024年员工持股计划,重点考核营收和创新药研发进度,彰显公司发展信心。2024年7月,公司为改善治理水平,调动骨干员工的积极性和创造性,吸纳高端人才,确保公司的核心竞争力的提升,确保公司发展战略目标与企业愿景的实现,发布了《2024年员工持股计划》。
该计划存续期为60个月,参与人数不超过46人(不含预留授予人员)――包括公司董事(不含独立董事)、监事、高级管理人员、中层管理人员、核心技术及业务骨干,认购的股票数量不超过551.00万股(含预留股份61.10万股),认购价格为6.68元/股。首次授予部分分三期解锁,解锁时点分别为自公司公告最后一笔标的股票过户至该员工持股计划名下之日起满12个月、24个月、36个月。
该员工持股计划首次授予部分考核年度为2024-2026年三个会计年度,每个会计年度考核一次,公司层面业绩考核目标选取营业收入(A)和创新药研发进度(B),解锁比例以营业收入(A)和创新药研发进度(B)的业绩完成度对应的解锁比例的孰高值为依据。2024-2026 考核年度,营业收入(A)的目标值分别为32.40亿元、36.00亿元、40亿元,触发值分别为29.16亿元、32.40亿元、36.00亿元,创新药研发进度(B)的目标值分别为2024年度创新药国内外IND批准数量不少于2个,或启动II期/III期临床试验不少于3个;2024-2025 年创新药国内外IND批准数量累计不少于4个且累计完成1个NDA受理,或启动II期/III 期临床试验数量累计不少于6个;2024-2026年度,创新药国内外IND批准数量累计不少于6个且累计完成2个NDA受理,或启动II期/III期临床试验数量累计不少于8个。
2.坚持以中药为基,化学仿制药为有益支撑
2.1.中成药是公司核心业务基础和重要增长来源
中成药是业务基石,管线丰富支撑公司稳步发展。公司持续拓展中成药销售市场,形成特色产品管线,主要治疗领域覆盖眼科、心脑血管、内分泌、呼吸、清热祛湿等,主要产品包括复方血栓通系列产品(核心品种)、脑栓通胶囊(核心品种)、复方丹参片、众生丸系列产品、清热祛湿颗粒等。

中成药是公司核心业务和重要收入来源,整体经营稳健,近两年受集采影响略微承压。若去除2020年外部环境影响,2018-2022年公司中成药销售规模稳健增长,从13.15亿元提升至16.34 亿元,CAGR为5.58%;2022年起核心产品陆续进入联盟集采、全国中成药集采,集采产品占2022年收入比重达51.35%,受集采产品降价影响,2023年中成药销售收入下滑至13.91亿元(同比-14.86%),随着集采执行基本落地, 2024年实现中成药销售收入13.18亿元,降幅收窄。随着集采影响逐步消解叠加公司销售策略调整与市场开拓,2025 年中成药板块经营有望回暖,集采“以价换量”效应逐步显现。
中成药策略多管齐下,助力板块向好发展。公司重点推动院内集采产品渠道下沉、构建零售业务培育核心品类、提升原有小份额产品市场贡献。通过核心产品复方血栓通系列制剂、脑栓通胶囊、舒肝益脾系列制剂、固肾合剂等持续拓展形成公司慢病治疗领域特色,为长期增长奠基;众生丸、清热祛湿颗粒从两广市场逐步布局全国。在多产品运营策略下,稳固基本盘,提升公司经营业绩。
2.1.1.复方血栓通系列产品:中成药集采承压,通过构建“量-本-费”协同增效模型以量补价
复方血栓通系列产品为公司核心品种,占据市场主导地位。复方血栓通系列产品属于国家基药目录、国家医保目录品种,主要剂型包括胶囊剂/软胶囊剂/颗粒剂/片剂。公司是复方血栓通系列制剂的产品原创者、标准制定者、行业引领者和市场主导者。复方血栓通胶囊是公司与中山医科大学眼科中心合作研制的中国第一个用于治疗眼底血管疾病的口服药物,是公司原研独家剂型品种,由三七、丹参、黄芪、玄参构成,具有活血化瘀、益气养阴功效,适用于眼底血管疾病、心脑血管疾病及糖尿病并发症的治疗,多年在国内眼科内服中成药领域位居市占率第一。

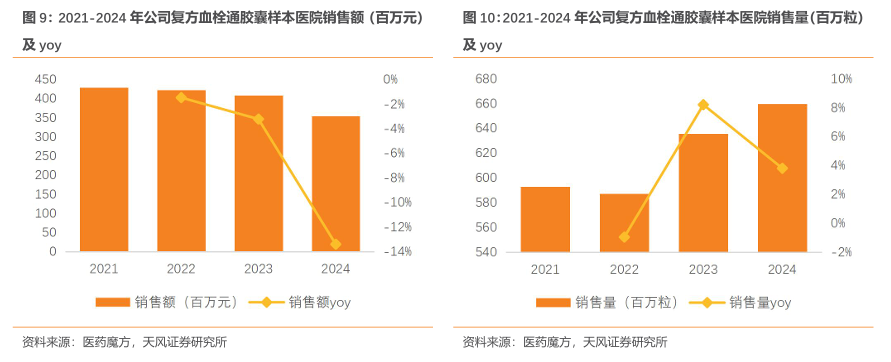
复方血栓通系列制剂集采降价导致销售规模下滑的影响主要体现在2023-2024年,2025年随着集采带动销量提升,有望实现恢复性增长:复方血栓通胶囊是公司销售TOP1的产品,根据医药魔方数据,复方血栓通胶囊2021年样本医院销售额实现4.28亿元。2022年,复方血栓通胶囊中选广东联盟牵头的六省中成药集采,中选价较2021年六省挂网均价降幅17.25%;2023 年 5月,复方血栓通胶囊中选全国30省/直辖市/自治区中成药集采,另复方血栓通软胶囊作为非代表品以同比例降价幅度随代表品中选,价格较前一年挂网价降幅38.59%。随着2023年-2024年广东联盟集采、全国中成药采购联盟集采的省份陆续执标最新价格,2023-2024年复方血栓通胶囊销售承压,样本医院销售额分别实现4.09亿元、3.54 亿元,同比下滑3.22%、13.39%。而从销量端看,2023-2024年样本医院复方血栓通胶囊销量均实现同比提升,分别为6.36亿粒(yoy+8.21%)、6.60亿粒(yoy+3.80%)。分析销售规模下滑的原因,我们认为主要是因为量增幅度短期未能弥补价格降幅。

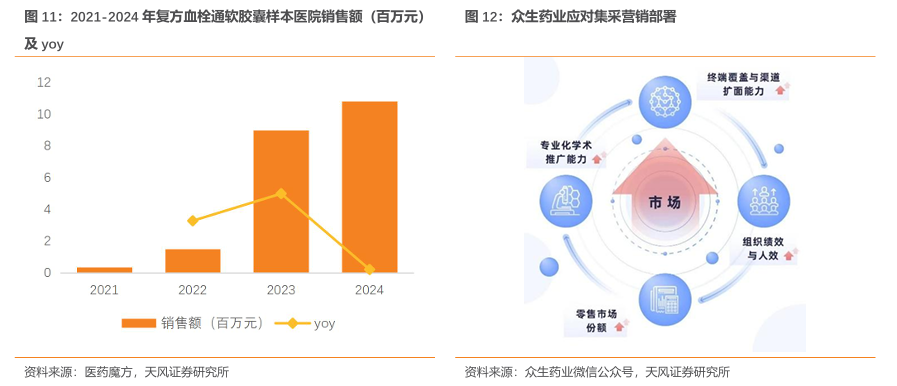
公司积极应对集采冲击,围绕核心产品构建“量-本-费”协同增效模型:销量增长扩大市场空间―通过工艺改进与供应链整合优化成本―以精细化费用管控体系,从而在集采价格下行背景下实现“以量补价”。具体方法包括:1)推动复方血栓通外延式渠道下沉,覆盖更多县级、基层和零售终端,提升市场份额;2)将复方血栓通系列产品作为整体进行营销布局,通过不同品规在各终端配合保持市场竞争优势,比如复方血栓通软胶囊在集采后实现销量快速增长,样本医院销售额从2021年35万元大幅提升至2024年1082万元;3)推动内部制度改革,激发营销组织活力。 2024年随着复方血栓通系列产品中选价格在全国中成药集采各省份陆续执标完成,集采降价影响基本出清,伴随着销量增长,2025年起有望实现恢复性增长。
2.1.2.脑栓通胶囊:加强循证医学研究,提升在心脑血管系统用药的核心竞争力
脑栓通胶囊是公司独家核心品种,脑血管用药市场拓展空间广阔。脑栓通胶囊是国家医保乙类品种、首家中药二级保护品种,由中国工程院王永炎院士基于“毒损脑络”病机学说研制的现代中成药,由蒲黄、赤芍、郁金、天麻、漏芦组成,用于缺血性脑卒中临床治疗,帮助患者改善脑血循环、保护神经功能、减少卒中残障。脑栓通胶囊属于心脑血管与血液系统药物中脑血管疾病治疗药,根据米内网数据,2024年心脑血管疾病中成药市场规模达755.90 亿元,其中脑血管疾病用药占比近四成,随着高龄化加深,脑血管中成药需求呈增长态势,市场空间有望进一步扩大。

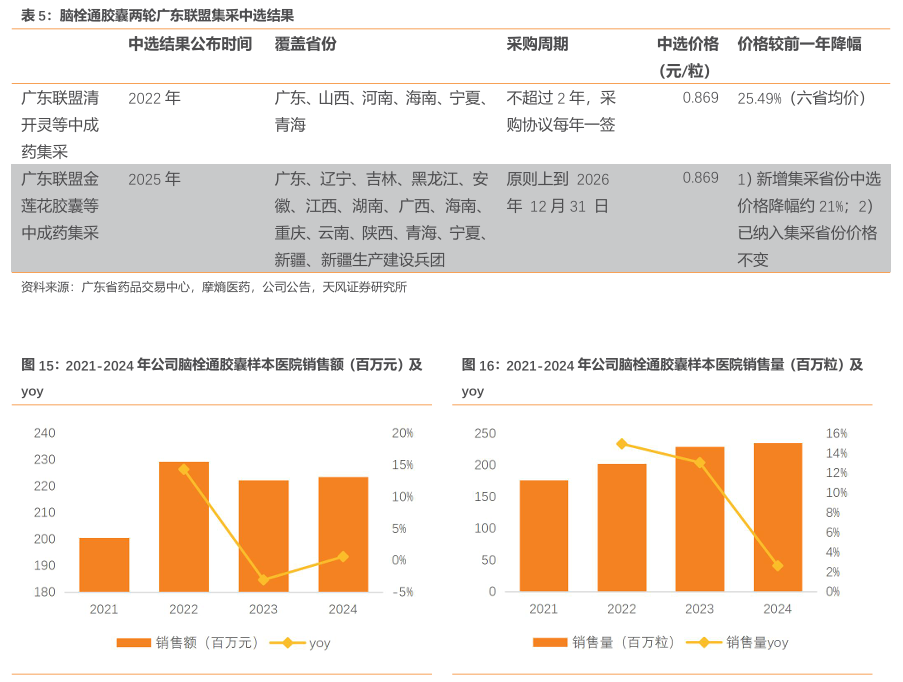
脑栓通胶囊纳入联盟集采,带动市场扩大销售放量。脑栓通胶囊2022年中选广东联盟清开灵等中成药集,中选价为0.869元/粒,较 2021年六省联盟的挂网价均价降价约25.49%,随集采落地执标脑栓通胶囊销售量增长显著,2023年样本医院销售量为2.29亿粒,同比增长13.07%;2024年销售量增长带动销售额企稳回升,实现样本医院销售额2.24亿元,说明集采带量对脑栓通胶囊销售放量影响积极.。2025年脑栓通胶囊中选广东联盟金莲花等中成药集采,集采覆盖范围从6个省份扩大到16个省份,随着集采省份扩容和落地指标,2025年有望扩展增量市场,实现销售提升。
2.1.3.公司布局中药管线研发工作,聚焦四大研发方向
公司积极开展中成药上市后再评价、推进中药休眠产品复产、探索布局中药经典名方及院内制剂开发以及拓展中药大健康领域。通过开展中成药上市后再评价,构建学术影响力和竞争优势,推动产品销量增长;通过推进中药休眠产品复产攻关,激活休眠品种市场价值,创造新的业绩增长点;通过积极探索布局中药经典名方及院内制剂开发,拓宽中药产品管线;通过积极拓展中药大健康系列产品设计与开发,实现中药健康类业务拓展。

2.2.坚持化学仿制药为有益支撑
化学仿制药是公司经营的有益支撑,公司积极参与国家集采和省际联盟集采,通过集采中选获得产品增量的市场机会。在化学仿制药方面,公司的头孢克肟分散片、头孢拉定胶囊、异烟肼片、盐酸乙胺丁醇片、吡嗪酰胺片、地夸磷索钠滴眼液在全国药品集中采购中中选,多个产品在省级集采或省际联盟集采中中选。
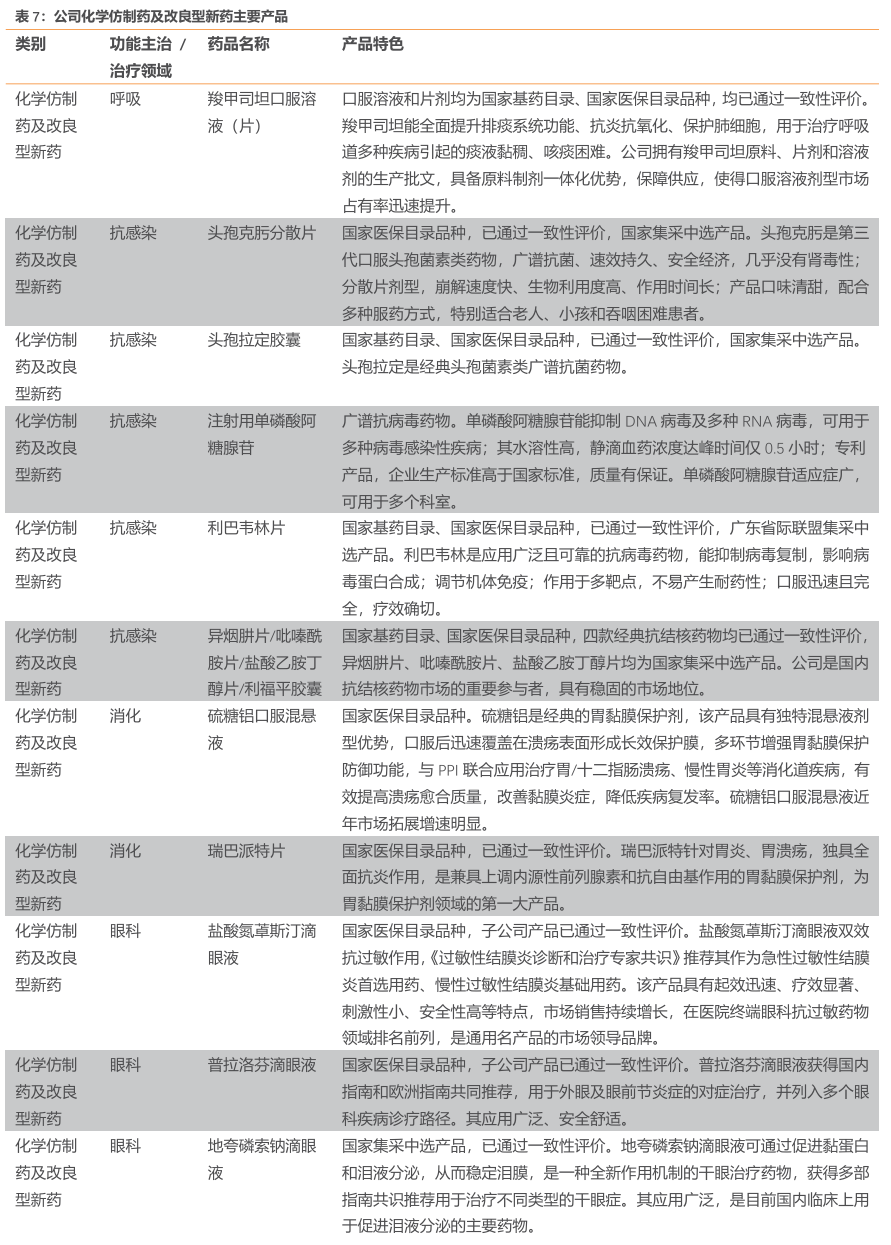

公司关注具有高技术壁垒特征的改良型新药,建立聚合物胶束载药平台,以该技术平台为依托,公司在研品种包括注射用紫杉醇聚合物胶束和注射用多西他赛聚合物胶束。公司将继续深入开展聚合物胶束、乳剂、缓控释制剂、复方制剂等改良型新药研究,丰富公司的创新能力和创新产品。
公司持续开展特色仿制药、高技术壁垒仿制药的研发,持续夯实现有滴眼液技术平台优势,稳步推进纳米乳剂、缓控释制剂、肠溶微单元制剂、儿童口服溶液制剂、多颗粒系统制剂、半固体制剂等技术平台打造。环孢素滴眼液(III)属于国内首家仿制获批上市,是国内首个通过豁免临床研究获批上市的仿制药眼用纳米乳剂。
3.坚持“创新引领”,布局呼吸系统及代谢疾病领域创新药
众生睿创为创新药研发及商业化平台,聚焦呼吸系统及代谢疾病领域。公司自2010年以来坚定向创新型制药企业方向迈进,2018年公司出资设立控股子公司广东众生睿创生物科技有限公司,专注于呼吸系统和代谢疾病领域创新药研发与商业化。
布局四大研发平台,创造良好的技术环境。公司持续加强研发平台建设,具有丰富的药品研发经验和高水平的专业技能。已形成小分子创新药研发平台、代谢性疾病新药研发与评价平台、抗病毒新药研发与评价平台、多肽创新药研发平台,为药物研发创造了良好的技术环境。
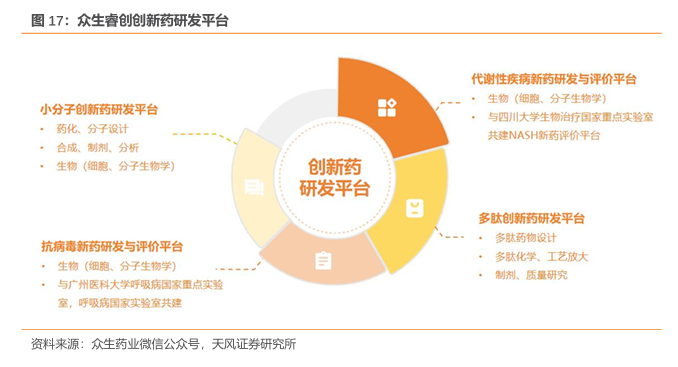
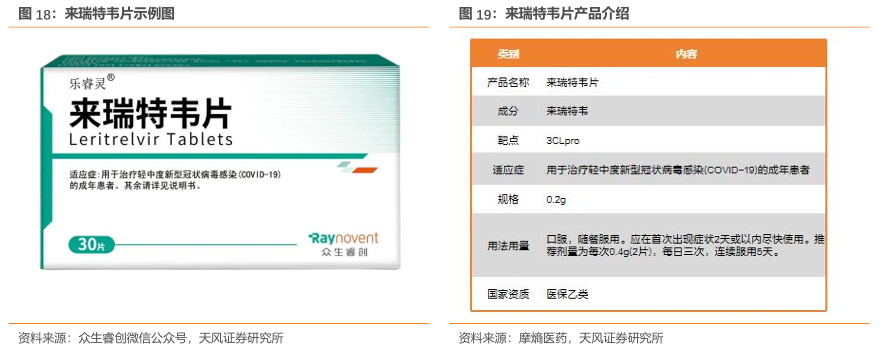
3.1.公司首款获批的创新药来瑞特韦片:3CL口服抗新冠单药,有效性安全性广受认可
来瑞特韦片(商品名:乐睿灵?,研发代号:RAY1216)是公司首款上市的一类创新药,为公司自主研发的中国首款具有自主知识产权的3CL单药口服抗新冠病毒感染的一类创新药物,已于2023年3月附条件批准上市,用于治疗轻中度新型冠状病毒感染(COVID-19)的成年患者,已纳入2023年国家医保目录乙类范围。
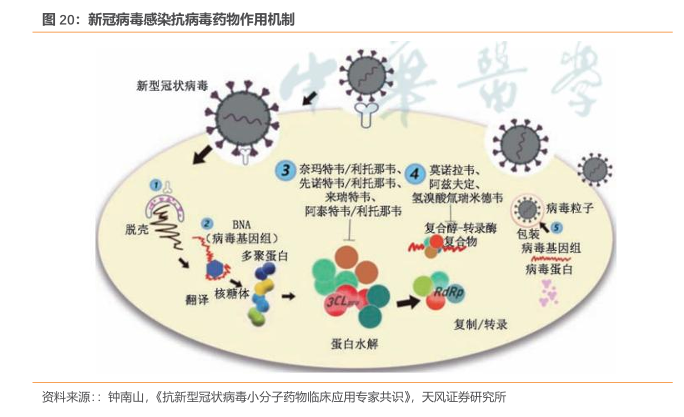
抗新冠病毒小分子药物作用机制是通过阻止新冠病毒复制治疗新冠病毒感染,包括3?胰凝乳蛋白酶样蛋白酶(又称主蛋白酶,3?chymotrypsinlikeprotease,3CLpro)抑制剂和 RNA依赖性 RNA聚合酶(RNA?dependentRNApolymerase, RdRp)抑制剂。
根据《抗新型冠状病毒小分子药物临床应用专家共识》,截至2024年3月4日,中国已获批上市7种口服抗新冠病毒小分子药物,其中3CLpro 抑制剂4种药物(奈玛特韦/利托那韦、先诺特韦/利托那韦、来瑞特韦和阿泰特韦/利托那韦),RdRp抑制剂3种药物(莫诺拉韦、阿兹夫定和氢溴酸氘瑞米德韦)
来瑞特韦片有效性和安全性广受认可:来瑞特韦片从基础机制研究到临床试验的学术研究成果已发表在国际顶刊自然杂志子刊《NatureMicrobiology》和国际权威期刊柳叶刀杂志子刊《eClinicalMedicine》,并已被列入《抗新型冠状病毒小分子药物临床应用专家共识》可用的国产小分子抗新冠病毒药物重点选择之一(证据质量A,推荐强度1)。
来瑞特韦片差异性竞争优势体现在其无需联用利托那韦作为增效剂,具备优秀的安全性及显著疗效,尤其适用于老年人及合并基础疾病的患者。
单药来瑞特韦是目前唯一一款无需联用利托那韦的 3CLpro 抑制剂。来瑞特韦不与利托那韦联合使用,药物相互作用相对较少且可控。而已上市的一些 3CLpro 抑制剂组合装存在利托那韦相关的药物相互作用风险。
《抗新型冠状病毒小分子药物临床应用专家共识》中推荐对有药物相互作用风险的老年患者在感染早期使用莫诺拉韦或来瑞特韦,建议对感染新冠病毒的肝、肾功能不全患者在感染早期优先选择莫诺拉韦和来瑞特韦。
相对于奈玛特韦,来瑞特韦与靶点相互作用更为广泛,形成的抑制复合物更加稳定,使得其靶点停留时间更长;对轻、中度新冠病毒感染成年患者有显著疗效,可以显著缓解临床症状、快速降低病毒载量、缩短病程及转阴时间。
3.2.全球First-in-Class 药物昂拉地韦ZSP1273:具备快速、强效、低耐药的核心竞争优势
公司自主研发的第二款创新药昂拉地韦片上市,进一步丰富了创新药产品线,提升核心竞争力。众生睿创研发的一类创新药昂拉地韦片(商品名:安睿威?,研发代号:ZSP1273)于2025 年5月22日正式获批上市。昂拉地韦是全球首个靶向甲型流感病毒RNA聚合酶PB2 亚基的抗流感药物,通过作用于甲型流感病毒RNA聚合酶的PB2亚基,抑制RNA聚合酶活性,从而抑制流感病毒复制,用于治疗成人单纯性甲型流感。
昂拉地韦片商业化方面,公司主要围绕“学术生态构建+数据化服务升级+关键项目实践”三大维度深化营销创新,目前已布局线下+线上销售渠道: 1)线下:2025年6月18日,昂拉地韦片在线下药店完成全国首单销售,启动药品供应,目前首批安睿威已进入广东省内多家核心医疗机构药房销售;2)线上:2025年6月底,昂拉地韦片已在京东健康线上首发,利用其全渠道优势提升可及性,覆盖线上购药需求。

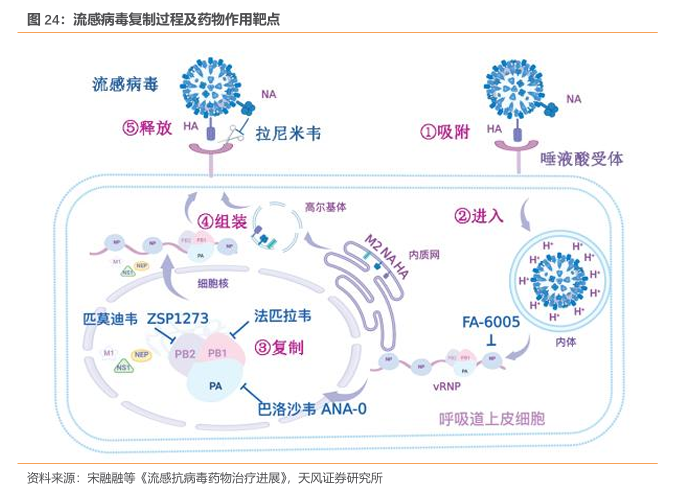
中国抗流感用药市场空间广阔,2023年仅奥司他韦一款药品销售近百亿。目前国内流感抗病毒药物市场奥司他韦占据主导地位,根据PDB数据,2023年销售98.63亿元,占比达86.48%。RNA 聚合酶抑制剂玛巴洛沙韦自2021年在中国上市以来,销售规模和市场占比逐渐提升,2021-2023年销售额从0.02亿元提升到6.27亿元,占比从0.07%上升至5.5%。根据头豹预测,中国抗流感药物市场规模有望到2028年提升至269亿,一方面在流感高发下推动抗流感市场快速扩容,一方面随着抗流感新药陆续上市或带来新的市场机会。
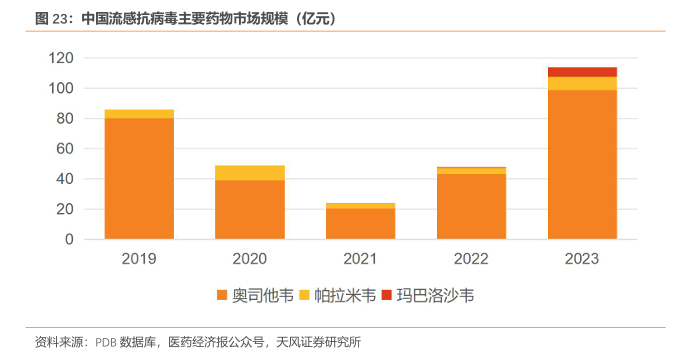
流感病毒是一种包膜病毒,结构自内而外为核心、衣壳和包膜,包膜分为内、外两层。内层为基质蛋白(M1),外层为脂质双层,镶嵌有两种突出表面的重要糖蛋白,分别是血凝素(HA)和神经氨酸酶(NA),HA在病毒进入宿主细胞过程中发挥作用,而NA则通过切割细胞表面的唾液酸,帮助子代病毒完成从宿主细胞的释放。流感病毒RNA聚合酶由3个亚单位组成,分别为聚合酶碱性蛋白 1(PB1)、聚合酶碱性蛋白(PB2)及聚合酶酸性蛋白(PA),在病毒复制中发挥关键作用。流感病毒生命周期需经历吸附、进入、复制、组装和释放过程,抗流感病毒药物分别在各阶段发挥作用。
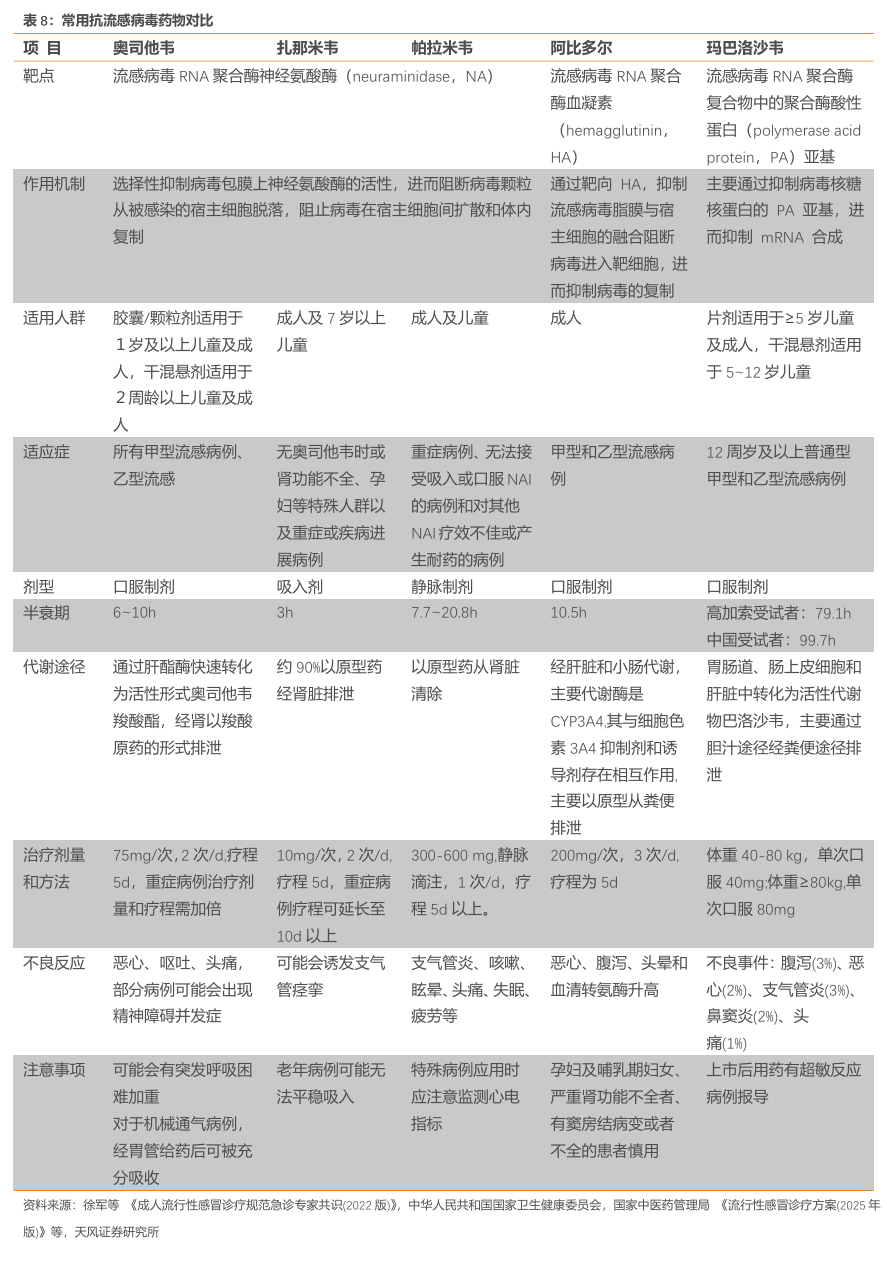
流感常用抗病毒药物根据作用制剂主要分为三大类:1)神经氨酸酶抑制剂NAI(奥司他韦、帕拉米韦、扎那米韦),通过抑制流感病毒NA活性起到抗流感病毒的作用;2)血凝素抑制剂HAI(阿比多尔),通过抑制流感病毒脂膜与宿主细胞的融合阻断病毒进入靶细胞,进而抑制病毒的复制;3)RNA聚合酶抑制剂(玛巴洛沙韦、法维拉韦、昂拉地韦),主要通过抑制病毒核糖核蛋白的PA亚基、PB1亚基或PB2亚基,进而抑制 mRNA 合成。其中RNA聚合酶抑制剂基于疗效好、安全性高、可用于治疗重症患者和耐药流感病毒株等优势,已逐渐成为抗流感新药研发重点。
流感治疗现有药物存在耐药率高、副作用大等不足:
奥司他韦:该药物在降低住院、肺炎或肺炎-中耳炎-鼻窦炎的复合症状发生的可能性方面缺乏确切证据。2017年WHO限制其仅适用于确诊或疑似流感重症住院患者引起的严重疾病的治疗,并不推荐预防性用药使用。在2008-2009年流感季期间,美国、日本等国报道甲型流感病毒(H1N1)对奥司他韦的耐药率已超过90%。
法维拉韦:仅用于其它抗流感病毒药品治疗无效或效果不佳时治疗成人新型或再次流行的流感,且有黑框警示具有生殖毒性(胚胎致死和致畸作用)。
玛巴洛沙韦:口服一次玛巴洛沙韦后发生耐药性突变比例为2.2%~23.4%,儿童患者发生耐药比例更高。由于流感病毒高突变率以及病毒之间重组现象的发生,已有的抗流感药物难以应对多变的流感病毒。
昂拉地韦片III期临床试验结果积极,显示出对奥司他韦的差异化优势。
III 期临床试验设计方案:采用多中心、随机、双盲、安慰剂或奥司他韦平行对照设计,设置昂拉地韦片600mgQD组、奥司他韦胶囊(达菲?)75mgBID组和安慰剂组,治疗方案持续5日,后续观察周期为21日,实际入组750例受试者。
Ⅲ期临床顶线数据表明:以七项核心流感症状(咳嗽、咽痛、头痛、鼻塞、发热/寒颤、肌痛/关节痛及疲劳)缓解时间为主要有效性终点指标,昂拉地韦组较安慰剂组显著缩短39%(P<0.001),较奥司他韦组亦缩短近10%。对比既往巴洛沙韦Ⅲ期临床试验结果,其较安慰剂仅缩短33%(P<0.001),而较奥司他韦组缩短不足1%。在重要的次要终点指标六项流感病毒学相关指标,昂拉地韦组相较安慰剂组/奥司他韦组均呈现统计学显著性差异。试验成功达成预期目标,证实该药物相较奥司他韦具备差异化优势。
昂拉地韦片具备快速、强效、低耐药的核心竞争优势:
快速:昂拉地韦可在给药后18小时内快速改善流感患者的全身临床症状。与安慰剂组相比,昂拉地韦可使七项流感症状缓解时间显著缩短24.52小时;
强效:昂拉地韦具备强大的抗流感病毒活性,其抗病毒效力显著优于奥司他韦和玛巴洛沙韦。昂拉地韦的EC90(抑制病毒90%最低有效浓度)为0.05nM,其抗病毒活性达到玛巴洛沙韦的50倍以上,是奥司他韦的1000倍以上。
低耐药:昂拉地韦对多种耐药病毒株均表现出很强的抑制活性,包括奥司他韦耐药株、玛巴洛沙韦耐药株及高致病性禽流感病毒株。此外,针对普通流感病毒,其抑制活性亦显著优于玛巴洛沙韦和奥司他韦。
昂拉地韦片的获批上市为流感治疗提供了新的药物选择,尤其适用于治疗选择有限或耐药风险较高的患者群体。

3.3.减肥药RAY1225:具备差异化竞争优势,看好海外授权潜力
3.3.1. GLP-1 市场持续增长,面临多个技术突破路线
GLP-1(R)类药物市场空间广阔,随减肥适应症获批有望带动市场快速放量。2025年全球GLP-1 药物市场规模达780亿美元,同比增长超50%,其中减重GLP-1市场规模达260亿美元,同比翻倍增长。分产品看,2025 年,替尔泊肽、司美格鲁肽销售额分别高达365.07亿美元、346.08 亿美元。其中,减重版替尔泊肽 Zepbound 销售额为 135.42 亿美元,同比增长 175%;减重版司美格鲁肽 Wegovy 销售额为 119.92 亿美元,同比增长 41%。
司美格鲁肽作为单靶点GLP-1受体激动剂,其减重效果已在STEP1研究中验证:在无糖尿病的肥胖患者(BMI≥30kg/m2)中,司美格鲁肽(2.4mg)联合生活方式干预68周后,平均体重较基线下降14.9%,显著优于安慰剂组的2.4%。
而替尔泊肽作为全球首款GIP/GLP-1双靶点激动剂,在头对头SURMOUNT-5试验中展现出碾压性优势:72周平均减重20.2%(约22.8公斤),显著优于司美格鲁肽的13.7%(约15.3 公斤)。临床试验的显著优势,直接转化为市场竞争力,截至2025年Q1,替尔泊肽在美国新处方量中的占比已达74%。
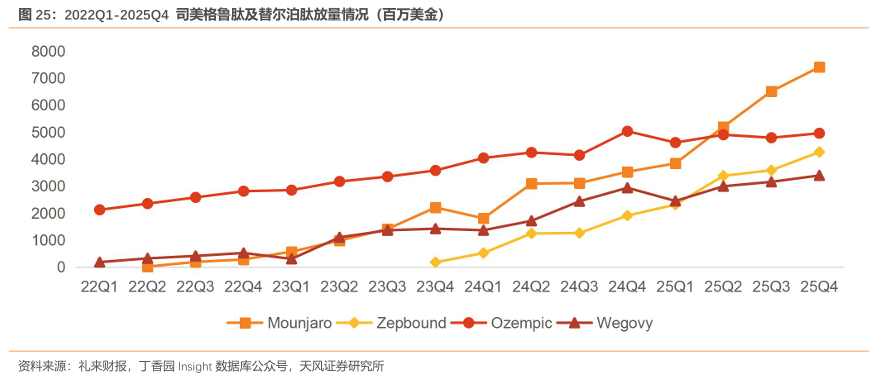
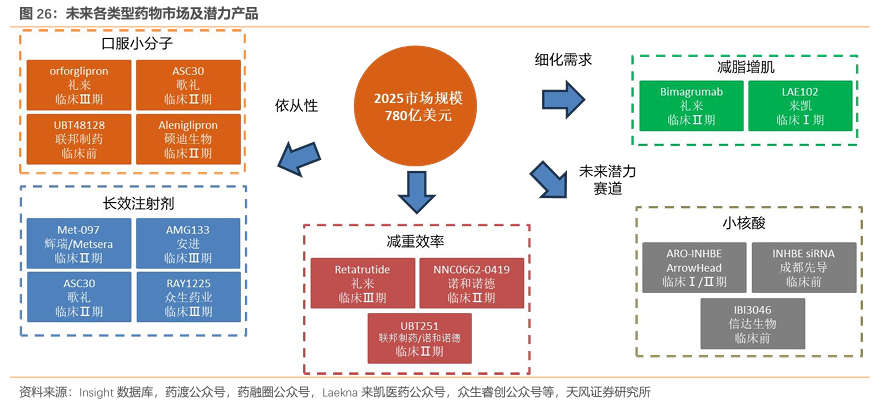
GLP-1 类药物目前销售额持续突破,但同时也面临着依从性、肌肉流失等问题,因此未来发展主要有以下几个方向:(1)口服小分子:目前已上市减重适应症的GLP-1产品给药方式均为注射,在依从性方面,患者更倾向于注射以外的用药方式。目前技术路线主要分为礼来和辉瑞2类,辉瑞因为安全性问题临床中止;(2)长效注射剂:此前辉瑞和诺和诺德就Metsera(其核心管线为长效amylin)并购展开激烈竞争;(3)减脂增肌:目前礼来的Bima、来凯的LAE102先后读出潜力数据;(4)小核酸:小核酸疗法直接干扰肥胖相关基因表达,兼具长效便捷、精准减重、与代谢性疾病共治这三大核心优势,有望成为未来的新modality;(5)减重效率:多靶点注射剂的减重效率持续突破,目前礼来的Retatrutide、诺和诺德/联邦的UBT251、诺和诺德的NNC0662-0419(GLP-1/GIP/AMYLN)有望角逐大体重减重细分赛道。
3.3.2.长效给药技术有望提高患者依从性和治疗效果
超长效给药技术的核心目标是延长药物在体内的作用时间,减少给药频率,目前主流技术包括纳米技术、微球技术、脂质体技术、融合蛋白技术和多肽偶联技术。在GLP-1类药物研发方面,以Metsera为代表的脂肪酸端基修饰技术、Amgen为代表的抗体偶联技术、以Camurus 与歌礼药业为代表的皮下储库缓控释技术、以众生药业、通化东宝为代表的肽钉合技术走在前列。
2025 年11月13日,辉瑞以92亿美元完成了对Metsera的收购,此次收购帮助辉瑞拿下了一系列潜力候选药物,包括即将进入III期临床的长效注射型GLP-1受体激动剂MET-097i,以及处于I期临床的长效胰淀素类似物MET-233i等。此外,礼来与诺和诺德也正积极布局,试图通过技术创新突破传统GLP-1类药物给药方式的局限,解决当前疗法的局限性,包括频繁注射、可扩展性限制、耐受性和疗效限制,实现药物的长效释放,从而提高患者的依从性和治疗效果。超长效给药技术的应用或将为减重赛道注入新的生命力。
1)脂肪酸端基修饰技术:Metsera的核心管线在于其超长效技术平台HALO,该平台将一个脂肪酸链修饰到候选肽药物的端基部分,使其能够可逆但紧密地结合血浆中的白蛋白,使得药物无需从白蛋白上解离也可以与GLP-1受体结合发挥作用,大幅延长了药物在人体内的半衰期。MET-097i在HALO平台上表现出约380小时的半衰期,支持每月一次给药。
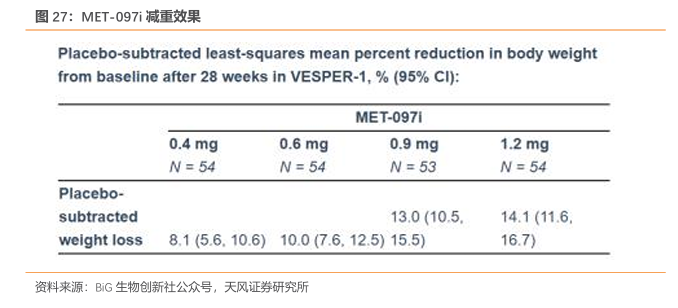
2024 年9月,MET-097i第I/II期试验的初步结果展现出极具竞争力且持久的减重效果,体重比基线下降7.5%,体重下降效果持续了至少8周。2025年9月,Metsera宣布MET-097i在IIb 阶段VESPER-1中28周实现了14.1%的双重激动剂样减重。
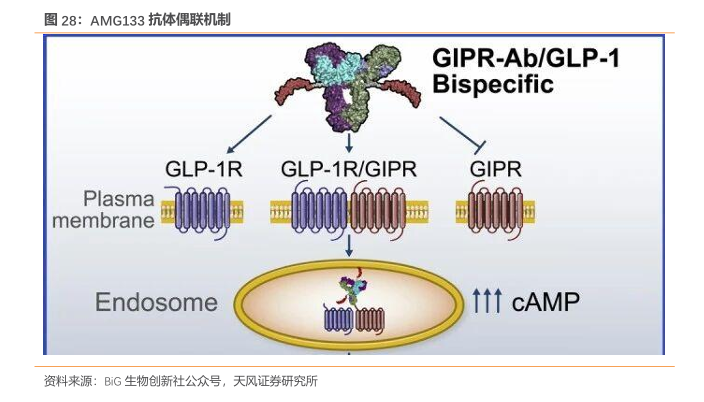
2)抗体偶联技术:安进的GIPR抗体融合GLP-1新药AMG133已进入III期临床阶段,其半衰期约为21天,约为食品药品监督管理局批准的每周一次治疗药物的最长效期药物的3倍,支持每月一次或更少频率的给药。II期临床结果中,每月一次的AMG133显著减轻了肥胖参与者的体重,肥胖组参与者平均体重减轻高达19.9%,肥胖糖尿病组参与者平均体重减轻最高达17.0%,最后一次给药后最长可维持减重效果到150天,同时心脏代谢指标也随之改善。
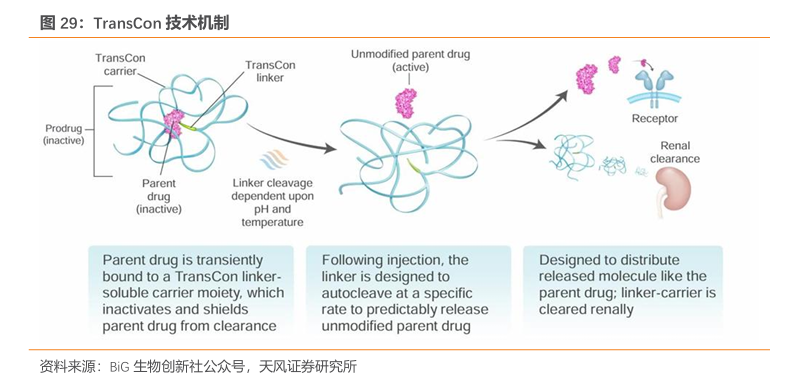
3)皮下储库缓控释技术:礼来与诺和诺德分别与Camurus与Ascendis达成战略合作,将利用它们的缓控释技术平台开发超长效管线。国内的歌礼制药也利用其皮下储库ULAP技术平台开发了多款超长效减肥药管线。Camurus的FluidCrystal平台核心是利用特殊的液体晶体材料,在体内可以形成稳定的药物储存库,药物从储存库中缓慢释放,达到长效作用。Camurus与诺和诺德合作,正开发基于此技术的司美格鲁肽月制剂改良新药CAM2056,目前已进入I期临床。Ascendis的TransCon技术利用前药系统,通过化学修饰将药物与惰性载体分子结合,形成稳定的前药复合物,在体内缓慢释放活性药物。2024年11月诺和诺德获Ascendis独家授权使用TransCon开发长效GLP-1受体激动剂。
4)肽钉合技术:肽钉合技术的核心是通过化学修饰将多肽链中的特定氨基酸残基连接起来,形成稳定的“钉合”结构。这种结构可以显著增强多肽的稳定性和生物活性,同时减少其在体内的降解和失活。同时肽钉合技术还可以结合其他化学修饰方法,如添加亲水性或疏水性基团,进一步优化多肽的理化性质和生物活性。
3.3.3. RAY1225:具备差异化竞争优势,已完成国内授权
公司在2025ADA大会上披露了RAY1225注射液两周一次治疗超重/肥胖参与者和2型糖尿病病参考者Ⅱ期临床试验的最新结果:
(1)REBUILDING-1,减重:
试验设计:REBUILDING-1研究采用剂量递增试验与扩展试验联合,交错启动剂量组的试验设计,包括RAY1225注射液3mg、6mg、安慰剂对照平行研究,和9mg及以上的剂量递增及扩展的安慰剂组内对照研究两部分,入组18岁及以上的超重或肥胖参与者。所有参与者均以滴定给药的方式接受24周皮下注射给药,每两周给药1次,共连续给药12次。此次大会中公布了3~9mg组有效性和安全性的阶段性结果,更高剂量组试验仍在进行中。
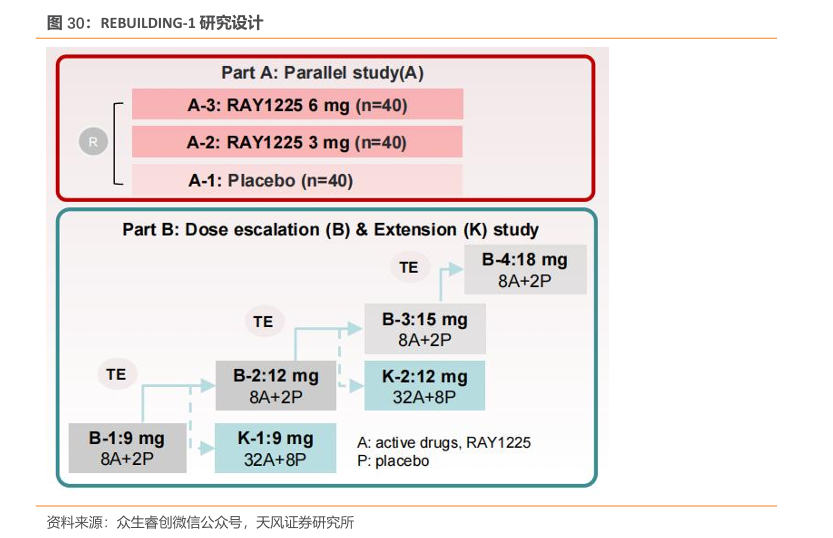
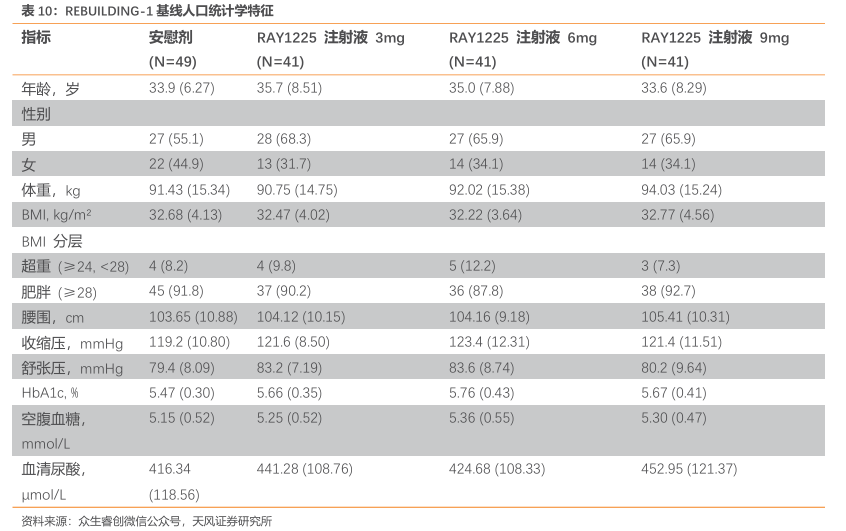
耐受性良好:RAY1225注射液在3~9mg剂量范围内,所有剂量组均表现出良好的耐受性,未发现新增安全性信号,整体安全性特征与既往临床试验和GLP-1类药物类似,相对缓慢的滴定过程让患者在治疗过程中能够更加舒适地接受药物治疗。
胃肠道反应轻:胃肠道不良反应是 GLP-1 类药物最常见的不良反应之一。在 REBUILDING-1 研究中,RAY1225 注射液引起的胃肠道不良反应严重程度大多较轻微,多发生在剂量滴定阶段,胃肠道不良反应的发生率低于同靶点药物替尔泊肽在中国超重或肥胖人群的Ⅲ期研究(SURMOUNT-CN)中的报道数据。其中,9mg组的腹泻、恶心、呕吐的发生率较替尔泊肽15mg组分别低11.5%、27.5%和9.9%,无患者因胃肠道不良反应停用药物。
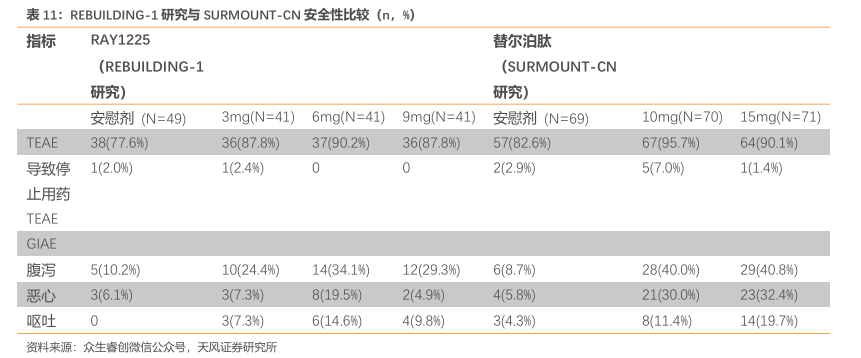
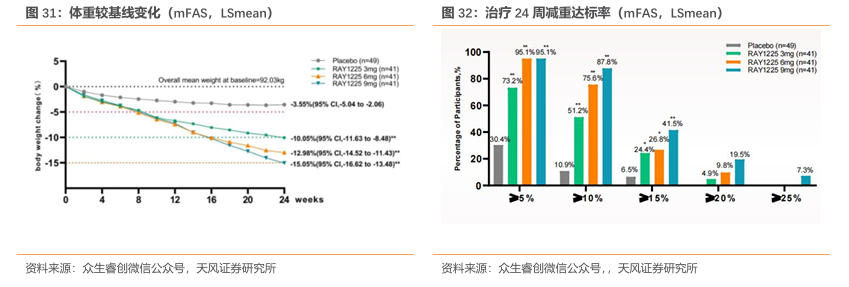
减重效果:RAY1225注射液3mg~9mg组每两周1次给药,治疗24周后体重降幅可达10.05%~15.05%。在减重达标率方面,3mg、6mg和9mg组体重较基线变化百分比≥5%的受试者比例分别为73.2%、95.1%和95.1%;各组减重效应均优于安慰剂组。RAY1225在更低剂量下就实现了与替尔泊肽相近甚至更优的减重效果,展现了其在减重治疗方面的潜力和优势。
心血管代谢生物标记物:RBUILDING-1研究设计 RAY1225在心血管和代谢相关指标(腰围、血压、血脂、血尿酸和肝酶、肝脏脂肪含量、空腹血糖和糖化血红蛋白等)中均展现出显著综合优势。能够更全面地改善患者的代谢状况,为患者带来更广泛的健康益处。
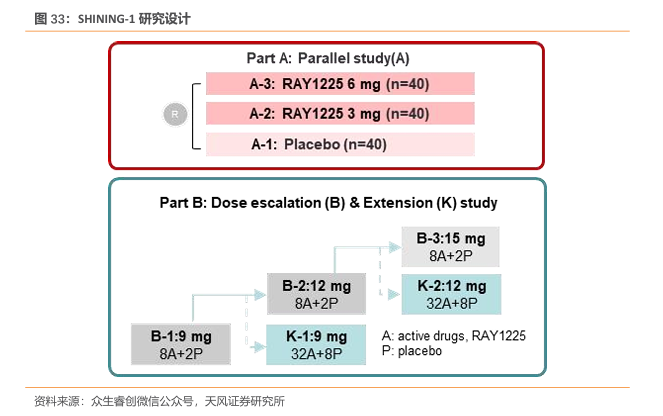
(2)SHINING-1研究,糖尿病:
研究概要:研究采用剂量递增试验与扩展试验联合,交错启动剂量组的试验设计,包括RAY1225注射液3mg、6mg、安慰剂对照平行研究,和9mg及以上的剂量递增及扩展的安慰剂组内对照研究两部分,入组18岁及以上的2型糖尿病患者。所有参与者均以滴定给药的方式接受24周皮下注射给药,每两周给药1次,共连续给药12次。
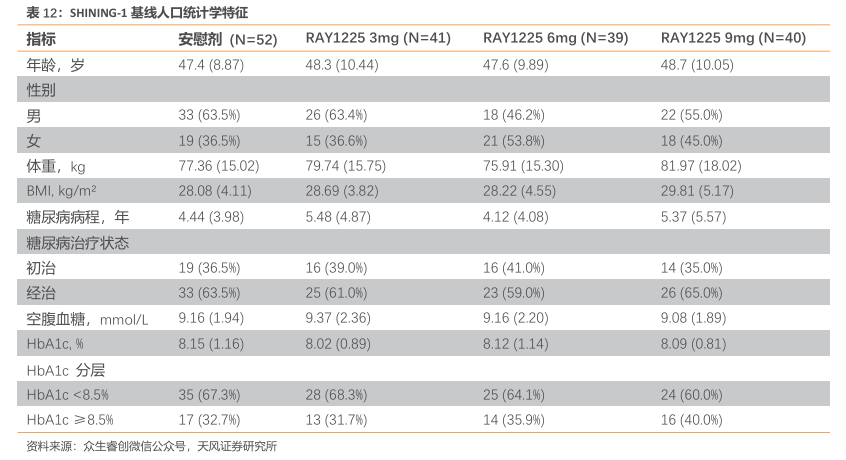
耐受性良好:RAY1225注射液在3~9mg剂量范围内,所有剂量组均表现出良好的耐受性,未发现新增安全性信号,整体安全性特征与既往临床试验和GLP-1类药物类似,相对缓慢的滴定过程让患者在治疗过程中能够更加舒适地接受药物治疗。
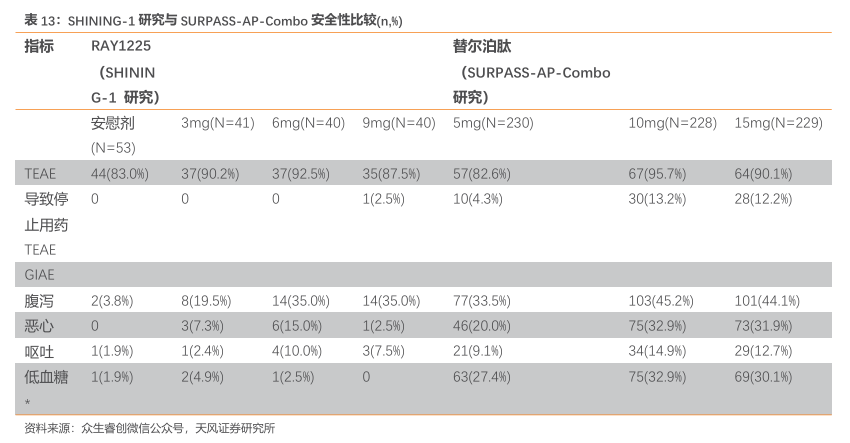
胃肠道反应轻:在SHINING-1研究中,RAY1225注射液引起的胃肠道不良反应严重程度大多较轻微,多发生在剂量滴定阶段。胃肠道不良反应的发生率低于同靶点药物替尔泊肽在以中国2型糖尿病人群为主的SURPASS-AP-ComboⅢ期研究中的报道数据。其中,9mg组的腹泻、恶心、呕吐的发生率较替尔泊肽15mg组分别低9.1%、29.4%和5.2%,无患者因胃肠道不良反应停用药物。
低血糖风险低:RAY1225注射液的低血糖风险较低,未发生严重低血糖事件。患者在使用过程中不必过度担心低血糖的发生,能够更安心地进行降糖治疗。
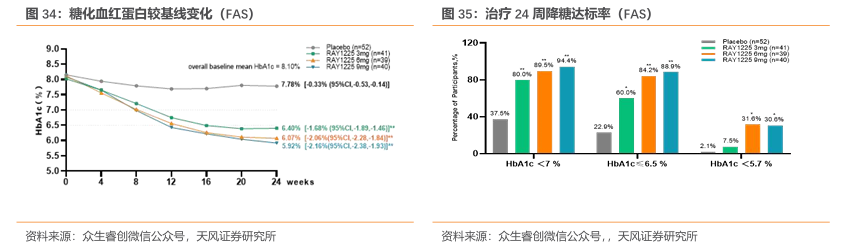
降糖效果:RAY1225注射液3~9mg每两周1次给药,治疗24周后糖化血红蛋白(HbA1c)较基线变化的最小二乘均数可达-1.68%~-2.16%,显著优于安慰剂组的-0.33%。降糖达标率方面,RAY1225 各组HbA1c<7%的达标率均≥80%;9mg组HbA1c<7%、≤6.5%和<5.7%的比例分别可达94.44%、88.89%和30.56%。与SURMOUNT-CN相比,RAY1225在更低剂量下就实现了与替尔泊肽相近甚至更优的降糖效果,展现了其在降糖治疗方面的潜力和优势。
综合代谢改善:除了在降糖方面的显著效果外,RAY1225注射液还对心血管代谢指标,如体重、腰围、血压、血脂和肝酶等方面有积极的影响,能够更全面地改善患者的代谢状况,为患者带来更广泛的健康益处。
截至2026年4月,公司国内2型糖尿病及肥胖均处于临床Ⅲ期,多个新适应症在申报过程中。2025年12月及2026年1月,公司2型糖尿病(经治)及2型糖尿病(初治)均完成全部患者入组,临床高效推进。
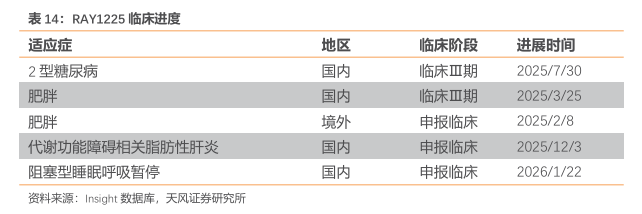
2026 年1月16日,公司与齐鲁制药举行战略合作签约仪式,宣布就创新药物GLP-1/GIP双靶点受体超长效激动剂RAY1225注射液签订许可协议,众生睿创授权齐鲁制药在中国地区(包括中国大陆、香港、澳门、台湾)内对RAY1225注射液进行生产与商业化销售,众生睿创保留许可知识产权的全部权利、权属和权益。在满足协议约定的条款下,众生睿创将获得首付款和里程碑付款总金额为人民币100,000万元,包括首付款人民币20,000万元、开发和销售里程碑最高合计人民币80,000万元,产品上市后有权获得许可产品净销售额双位数的销售提成。同时,众生睿创将继续负责推进相关适应症在合作区域的临床开发和注册等工作。
本次合作有助于发挥众生睿创RAY1225注射液领先的产品优势和齐鲁制药强大的商业化优势,进一步加速未来RAY1225注射液在中国地区的商业化进程,有效满足国内巨大的临床需求。
3.4. First-in-Class 药物 ZSP1601:用于 MASH 治疗,处于IIb期临床试验阶段
ZSP1601 片是众生睿创研发、国内首个获批临床用于治疗代谢功能障碍相关脂肪性肝炎(MASH)的一类创新药,是一种泛磷酸二酯酶(PDE)抑制剂,具有全新作用机制和全球自主知识产权的First-in-Class 药物。目前正在开展IIb期临床试验,2024年12月参与者入组已完成。

MASH治疗市场前景广阔,对应治疗药品需求待满足:非酒精性脂肪性肝病(NAFLD)是遗传易感个体由于营养过剩和胰岛素抵抗引起的慢性进展性肝病,疾病谱包括非酒精性脂肪肝(NAFL)、非酒精性脂肪性肝炎(NASH)及其相关纤维化和肝硬化。NASH属于坏死性发炎过程,肝细胞由于脂肪累积而受到损,可导致肝脏般痕,可能会发展为肝硬化及肝癌。在2023年EASL年会上,非酒精性脂肪性肝病(NAFLD)、非酒精性脂肪性肝炎(NASH)分别更名为代谢功能障碍相关的脂肪性肝病(MASLD)、代谢功能障碍相关的脂肪性肝炎(MASH)。
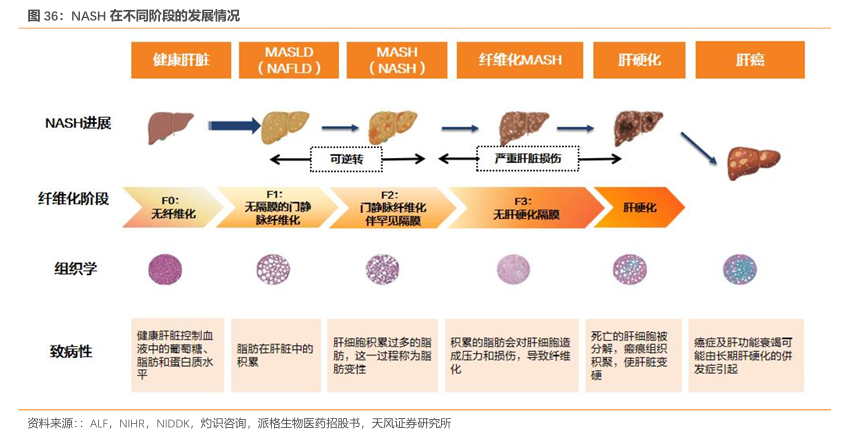
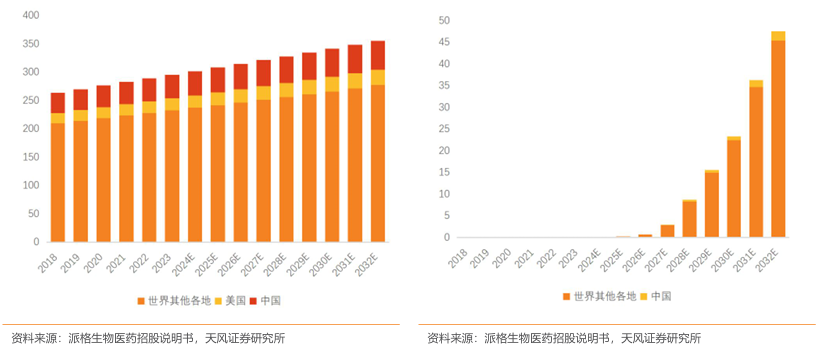
MASH已成为全球性的健康问题,患病率逐年上升。2023年全球/中国MASH患病人数分别达2.96亿人、4150万人,预计到2032年全球将有3.56亿MASH患者,其中中国患病人数达5080万人。而MASH由于多通路治病机制、靶点验证难度高,药物研发难度较大,目前全球仅2款以MASH为适应症的药品上市,一款为2020年上市的全球首个治疗MASH的药物Saroglitazar(PPARα/γ双重激动剂),但仅在印度获批,未得到广泛使用;一款为2024 年 3 月 FDA 获批上市的甲状腺激素受体β-选择性激动剂resmetirom(商品名:Rezdiffra),用于治疗患有中度至晚期肝纤维化的MASH患者,被广泛认可为首款治疗MASH的药物,标志着MASH治疗进入新阶段。根据灼识咨询预测,2032年MASH药物市场规模将达476亿美元,其中中国市场规模为22亿美元。
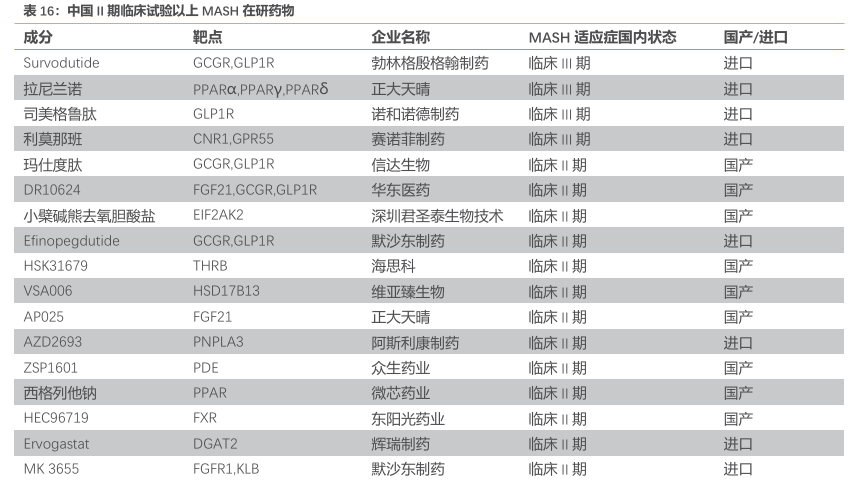
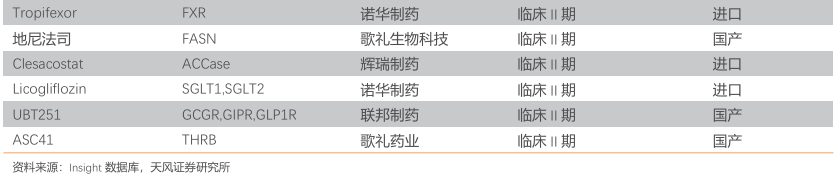
公司已布局2款MASH治疗药物,其中ZSP1601在国产药物中进度靠前。中国MASH药物研发活跃,但大多数企业仍处于早期研发阶段,批准临床和临床I期数量最多。中国MASH药物研发靶点众多,较为集中在THRB、FXR、GLP-1R靶点。公司在MASH治疗领域共布局2款药品,ZSP1601(适应症为MASH治疗)、RAY1225(适应症包括减重、降糖、MASH治疗),具备数量优势,且ZSP1601在国产在研MASH药物中进度靠前(目前国内23款MASH治疗药品处II、III期临床试验阶段,其中国产研发进度靠前的有12家均处于II期临床试验阶段,ZSP1601为其中之一)。
风险提示
行业风险,研发风险,国内市场竞争风险,股价异动风险