
近日,荣昌生物发布2022年三季度业绩公告,前三季度实现营收5.7亿元,同比增长397%;归母净利润-6.88亿元。
与业绩大幅亏损相反的是,荣昌生物在A股科创板的表现可谓亮眼,截至10月28日,股价已较今年四月上涨超150%。

荣昌生物科创板走势
自去年7月以来,《以临床价值为导向的抗肿瘤药物临床研发指导原则》引发业内对创新的冷思考,被资本簇拥5年之久的创新药突然步入寒冬,大量Biotech上市即破发。寒冬之下,多数Biotech都在挣扎求生,荣昌生物却能成功实现“A+H”两地上市,并持续获得资本青睐,其内在逻辑值得国内Biotech思考借鉴。
1
两大核心FIC,商业化全面提速
一款新药的上市需要“十年十亿美元”,然而对于Biotech而言,研发产品上市只是第一步,或许还是最容易的一步,商业化是一款新药的“试金石”,更是摆在Biotech和Pharma之间难以逾越的门槛。
荣昌生物正在实现商业化的两大核心产品分别是泰它西普和维迪西妥单抗。
泰它西普是一种全球首款、同类首创的BLyS/APRIL双靶点新型重组TACI-Fc融合蛋白产品。目前在自身免疫疾病领域共有7个适应症处于商业化或临床试验阶段。
其中系统性红斑狼疮(SLE)适应症于2021年3月获批在国内上市销售,是近60年来第二个获批的系统性红斑狼疮治疗领域的新药。
2021年12月,泰它西普被纳入国家医保药品目录用于治疗SLE。截至2022年6月30日,荣昌生物自身免疫商业化团队涵盖全国31个省级行政单位的241个地级市的1021家医院,已准入337家医院,及717家双通道药房。
维迪西妥单抗是一款新型抗 HER2 ADC 产品,是中国首款自主研发的ADC创新药、目前唯一一款获得美国 FDA授予突破性疗法认定的中国ADC产品。
其用于治疗胃癌、尿路上皮癌的新药上市申请经优先审评审批程序,并作为具有突出临床价值的临床急需药品分别于 2021年6月、2021年12月在中国获附条件批准上市,填补了ADC药物在尿路上皮癌、HER2低表达肿瘤治疗领域的空白。
2021年12月份,维迪西妥单抗被纳入国家医保药品目录用于治疗HER2表达局部晚期或转移性胃癌(GC)。2022年上半年,荣昌生物肿瘤科商业化团队涵盖全国29个省级行政单位的185个地级市的887家医院。截至2022年6月30日,肿瘤商业化团队已准入340家医院。
维迪西妥单抗
来源:公司官网
两大核心产品被纳入医保后,虽然价格分别下降68.34%和71.85%,但产品可及性大幅提升,产品销量显著提高。
从销售数据来看,今年上半年,荣昌生物实现总营收3.5亿元,同比增长1033.35%,除去0.2亿元的技术授权收入,已上市的两款药物销售收入3.29亿元,同比增长242%,占总营收比重高达93.8%。
三季度虽未公布收入类型,但在国内疫情反复的背景下,单季度实现销售额2.19亿元,同比增长162.3%,环比增长9.5%,业绩表现超出预期。
新药商业化拓展顺利的背后,是荣昌生物前瞻性的布局,早在3年前就着手组建国内商业化团队。2020年-2022年三季度,荣昌生物的销售费用分别为2418万元、2.63亿元及2.78亿元,对应5.7亿的销售收入,占比为48.8%,这对于正在拓展市场的新药而言较为高效。
比较来看,相比于其他Biotech公司,荣昌生物为商业化做了更充足的准备,核心产品商业化拓展更高效。在从Biotech向Biopharma迈进的第一年,交出一份亮眼成绩单的同时,为后续创新提速奠定夯实基础,向资本市场传递了其潜在的持续盈利能力。
2
三年“烧”18亿,管线梯队储备丰富
资料显示,2020年-2022年前三季度,荣昌生物的研发费用分别为4.66亿元、7.11亿元以及6.63亿元,分别同比增长32.31%、52.63%及26.29%,三年不到,累计研发投入18.4亿元。
研发投入的增加,意味着其研发管线不断进入临床阶段。截至目前,荣昌生物共布局了抗体融合蛋白、ADC、单抗及双抗药物三大管线,覆盖自身免疫性疾病、肿瘤和眼科三大领域,开发了20余款候选生物药产品,其中10余款候选生物药产品处于商业化、临床研究或IND准备阶段。
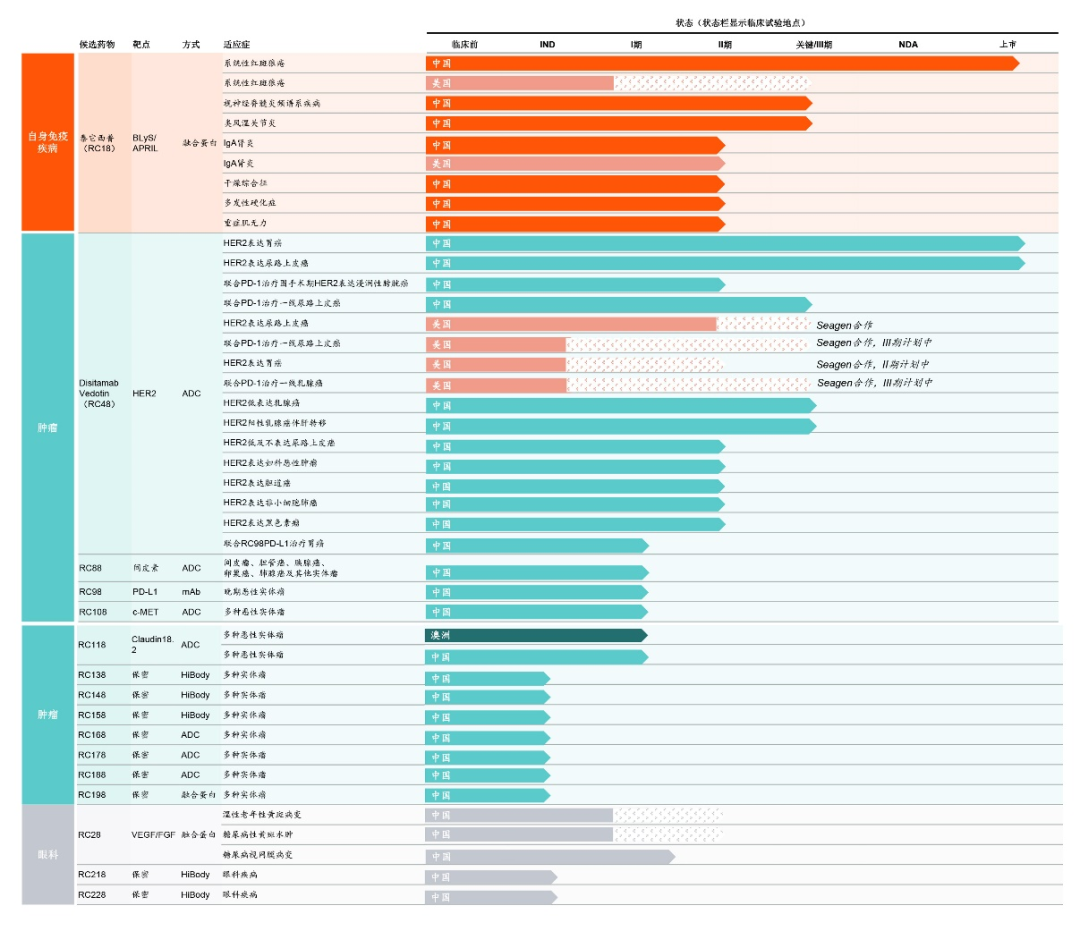
荣昌生物研发管线
来源:公司官网
其中,泰它西普和维迪西妥单抗除了已获批的三大适应症外,还在不断拓展其他具有市场竞争力的重磅适应症。
泰它西普方面,正在就治疗多种自身免疫性疾病进行多项临床试验,包括用于治疗视神经嵴髓炎(NMOSD)、类风湿关节炎(RA)、干燥综合征(SS)、IgA肾病、多发性硬化症(MS)和重症肌无力(MG)等的Ⅱ/Ⅲ期临床试验,预计将陆续于2024年-2027年获批。
维迪西妥单抗方面,正就治疗多种实体瘤进行临床试验,包括胃癌、尿路上皮癌、乳腺癌、非小细胞肺癌、胆道癌、妇科恶性肿瘤、晚期黑色素瘤等。此外,荣昌生物还在探索维迪西妥单抗联合PD-L1治疗HER2表达局部晚期或转移性实体瘤的临床可能性,预计将于2024年-2027年获批。
除此以外,荣昌生物通过其领先同行的三大技术平台(抗体和融合蛋白平台、 ADC平台、双抗平台),持续推出产品矩阵。
在抗肿瘤领域,布局了RC88、RC98、RC108、RC118等11款产品,覆盖PD-L1、ADC和融合蛋白等多种药物类型。眼科疾病领域,布局了RC28、RC208、RC218和RC228等四款在研产品。
其中,RC28是一款VEGF/FGF双靶点的创新融合蛋白产品,用于治疗多种眼科疾病处于临床研发阶段,有望成为“first in class”的VEGF/FGF双靶点眼科生物药。
相比于其他已上市或在研的单靶点VEGF抑制剂产品,RC28能更有效地抑制多种眼部疾病有关的眼底血管新生,提供包括减少用药剂量、降低用药频率、降低治疗成本、提升患者依从性等更优的治疗方案,进一步改善患者生活质量并提升整体疗效和安全性。
持续高额的研发投入需要巨额的资金储备。得益于在港股和A股市场上募集的资金,荣昌生物目前的现金储备十分充足。
三季报显示,荣昌生物期末现金及现金等价物余额高达19.7亿元,另有大量理财产品。这为研发管线的持续推进及已上市产品的国内外商业化提供了充足的现金流支持。无需担心出现类似其他Biotech,因资金不足而被迫砍掉或出售研发管线的困难局面。
3
股权激励,目标“160亿”
为将公司长远发展与核心员工个人利益绑定,10月17日,荣昌生物发布了A股限制性股票激励计划(草案):拟向188名员工授出358万股,授予价格为36.36元。其中,首次授予A类权87.305万股,B类权益199.64万股,合计286.945万股;预留71.055万股。
通过这份激励计划的业绩考核目标,可以看到荣昌生物对公司未来发展的信心。
根据激励计划,首次授予部分的业绩考核目标为,若要达成业绩考核目标A,则2022-2026年度的累计营业收入依次为7.5亿元、20亿元、40亿元、70亿元、110亿元(营业收入以合并报表所载数据为计算依据,不包括泰它西普的海外授权收益,下同),累计启动临床试验依次为6个、12个、20个、28个、36个。
预留授予部分的业绩考核目标为,若要达成业绩考核目标A,则2023-2027年度的累计营业收入分别为20亿元、40亿元、70亿元、110亿元、160亿元,累计启动临床试验依次为12个、20个、28个、36个、44个。
这意味着荣昌生物未来五年的营业收入需要保持每年至少40%的增长速度,且每年需要新启动临床试验8个。
荣昌生物的信心来源,一方面是随着泰它西普和维迪西妥单抗更多适应症的获批,两大核心产品带来了业绩高确定性。
另一方面,国际化稳步开展,更大市场范围内的商业价值正在变现。泰他西普在美国启动的针对SLE的国际多中心III期临床研究、针对IgA肾病适应症的II期临床试验正在稳步推进,并获得美国FDA颁发的针对MG治疗的孤儿药资格认定;就维迪西妥单抗与Seagen达成合作协议,获得高达26亿美元的首付款和里程碑付款、外加最高超过15%的梯度销售提成。
此外,在规模化生产方面,荣昌生物已建立符合全球GMP标准的生产体系,包括21个2000升一次性袋式生物反应器在内的细胞培养、纯化、制剂及罐装等生产车间及配套设施,并计划在2025年末将原液总产能扩大至80000升以上。

荣昌生物生产设备
来源:公司官网
整体而言,荣昌生物差异化的产品管线、前瞻性的国际化布局、以及稳步推进的产业化项目,让其未来的业绩充满确定性,有望成为为数不多从Biotech成功转型Biopharma的代表。
4
结语
没有人知道寒冬将持续多久,但资本不会撒谎,能够从寒冬中活下来的创新药企,必然是真正具有竞争力、最有发展潜力的。荣昌生物作为中国生物药界的“新贵”,展现出来的商业潜力,值得期待。